血管内皮生长因子(Vascular Endothelial Growth Factor , VEGF)在血管生成(angiogenesis)、血管通透性调节以及细胞增殖和存活中起关键作用,主要效应细胞为内皮细胞(ECs)[1]。VEGF家族包括VEGF-A/B/C/D/E、胎盘生长因子(PIGF)共6个成员,根据其外显子剪切的不同,主要分为5种亚型,再根据氨基酸的长短依次命名为VEGF145、VEGF165、VEGF121、VEGF189、VEGF206,其中VEGF165是最常见且生物活性最强的亚型之一,也是内皮细胞分泌最活跃且分布最广泛的因子[2]。
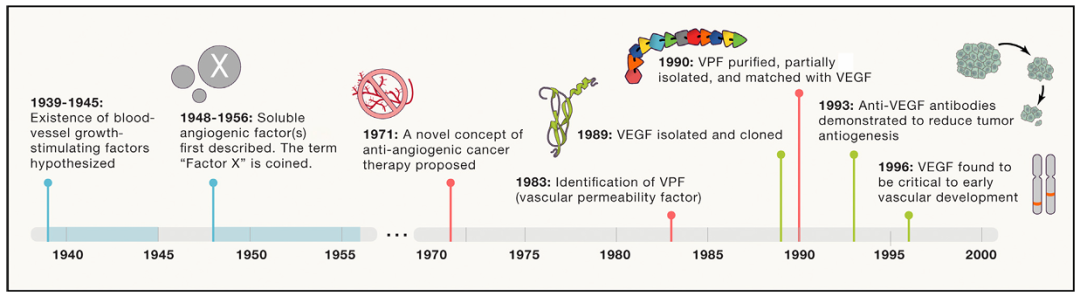
VEGF发现历史[1]
VEGF165通过与细胞表面的受体(如VEGFR-1/23)结合,激活下游信号通路,在促进血管生成、组织修复、胚胎发育过程中发挥重要作用。
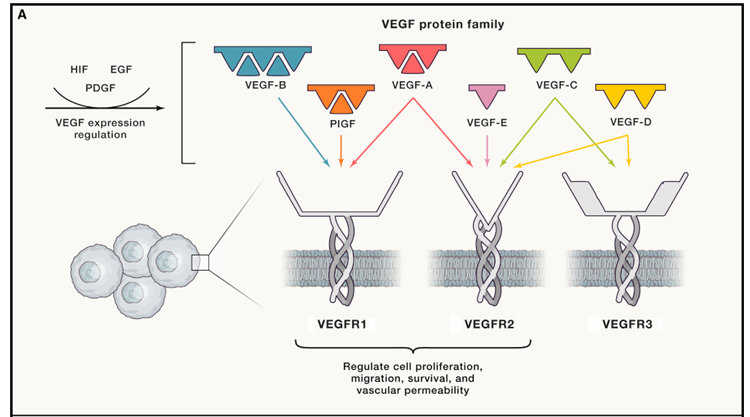
VEGF的激活和信号[1]
毛囊干细胞诱导分化血管内皮细胞[2]
2017年,浙江中医药大学附属江南医院的研究者在J Cell Mol Med期刊上发表了一篇论文,该研究通过VEGF165诱导毛囊干细胞(rHFSC)分化为内皮细胞,为了进一步论述实验的可靠性,作者通过裸鼠体内验证了新生血管的生成,设计了3组实验(PBS + Matrigel、VEGF165 + Matrigel、VEGF165 + rHFSCsGFP + Matrigel),结果证明PBS + Matrigel组几乎没有血管形成,VEGF165 + Matrigel组表现出形成血管的能力且有新生血管,VEGF165 + rHFSCsGFP + Matrigel)组具有明显的新生血管网络。总之,该研究改进和优化了rHFSC的分离、培养和纯化方法,并建立了诱导 rHFSCs分化为内皮细胞的方法,并在体内探究了体内促血管生成的过程,为血管构建、血管成形术和伤口早期血管形成提供了理论基础,并为使用组织工程皮肤临床治疗缺血性疾病提供了新的见解。
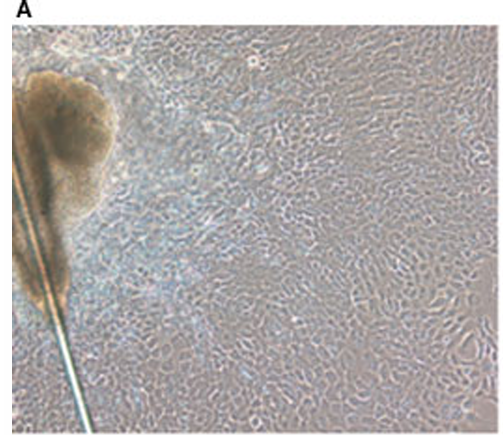
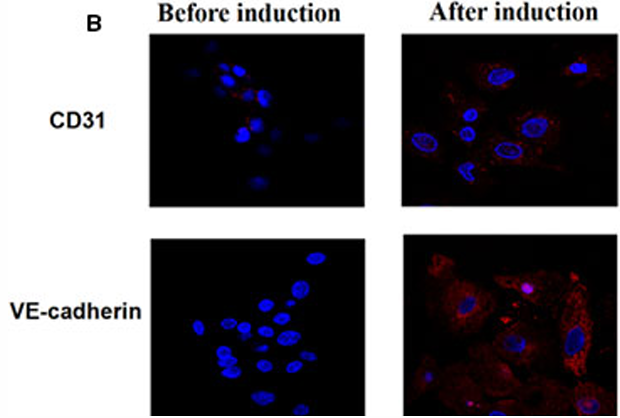
图1 A-原代毛囊干细胞 B-VEGF165诱导后血管内皮标志物对比
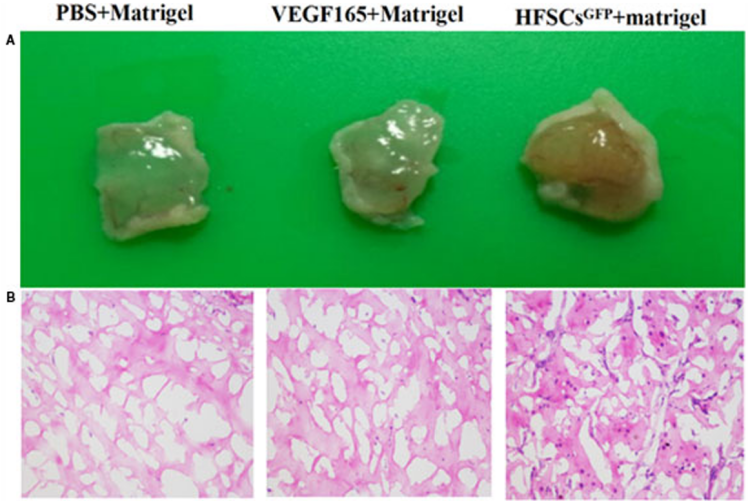
图2 裸鼠体内新生血管验证
iPSC诱导分化为血管内皮细胞[3]
内皮细胞(EC)排列在血管内壁上,调节血管张力、结构和炎症。ECs对于维持血管稳态至关重要,ECs功能障碍在驱动动脉粥样硬化和高血压等普遍的血管病变中起着关键作用。由于原代人ECs难以获得,可塑性和增殖能力有限,因此相比之下,iPSC为各种应用(包括疾病建模、细胞治疗、组织移植血管化和微生理系统)生成EC提供了潜在的无限来源。
2021年,国外一篇研究通过VEGF165诱导法建立了由iPSC生成血管内皮(viEC)的方案,经过7天的时间,将从350万个人iPSC中分化多达5500万个血管内皮细胞(viEC),并对生理剪切力下的血管内皮细胞的行为进行了研究。该方案产生的viEC表现出内皮细胞的多种特征功能,包括EC标志物表达、流向对齐、敏感基因的上调等,生成的内皮细胞可产生一氧化氮,响应内皮一氧化氮合酶 (NOS3) 反应,以维持血管稳态。
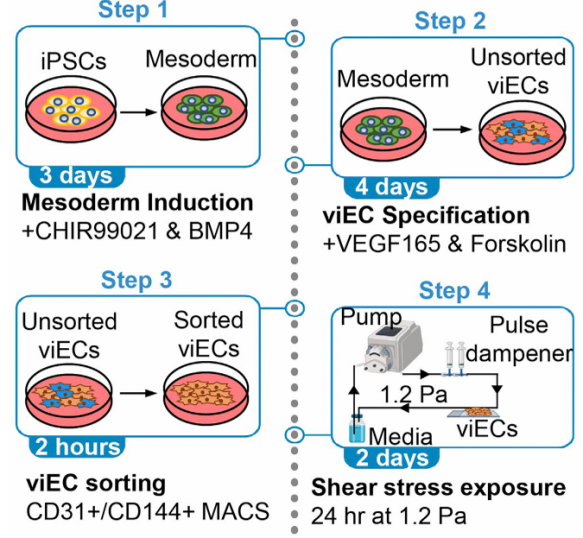
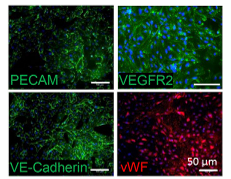
图3 实验设计示意图(左) ECs标记物(右)
血管化前沿进展

自2009年研究者对血管化技术的首次探索,经过近20年的发展历程,虽然已成功构建多种血管化类器官模型,但通常缺乏清晰、完善的血管系统,对自组织血管网络形成的机制探究极为匮乏。
近日,国外专家于顶刊Science上发表了一篇重磅论文,该报道从人多能干细胞(hPSCs),在多种血管化诱导因子VEGF/FGF2/PDGF-BB/TGF-β1等的作用下,首次在体外构建了与6.5周人类胚胎心脏发育阶段相似的心脏血管类器官(具有心肌细胞、内皮细胞和平滑肌细胞),精确模拟了人类胚胎发育早期心脏的血管形成过程[4]。
该研究不仅构建了兼具血管功能和结构的血管化类器官,也证明了血管生成机制可能是保守的,该研究结果不仅可用于体外心血管机制的深入探索,并且具有可预见的普适性,不仅对于类器官技术的发展具有关键推动作用,也为发育生物学、先天缺陷疾病建模带来新的突破。
内皮细胞在血管生成、血管形成和分化过程中起着至关重要的作用,特别是在血管内皮细胞分化和血管化类器官构建中。VEGF165是诱导iPSC向血管内皮细胞(Endothelial Cells, ECs)分化的关键因子,可以显著提高iPSC分化的效率以及血管生成,因此,在心脏、肝脏、肾脏等器官的类器官培养中,VEGF165有助于类器官血管网络的形成和功能成熟,为组织工程、再生医学和疾病模型研究提供强有力的工具。
hPSC诱导类器官培养工具书,纸质版免费限时申领

-
9大hPSC来源类器官实验流程
-
提供经验证的细胞因子种类和使用浓度
-
所需培养试剂组合推荐搭配
扫码申请《hPSC诱导类器官白皮书》

近岸蛋白可提供高活性、高批间一致性的血管生成相关培养因子,包括VEGF165、FGF basic,、PDGF、 ANG、PGF、CXCL趋化因子等,覆盖人属、鼠属,助力体外血管化技术的研究与发展。
VEGF165批间一致性数据
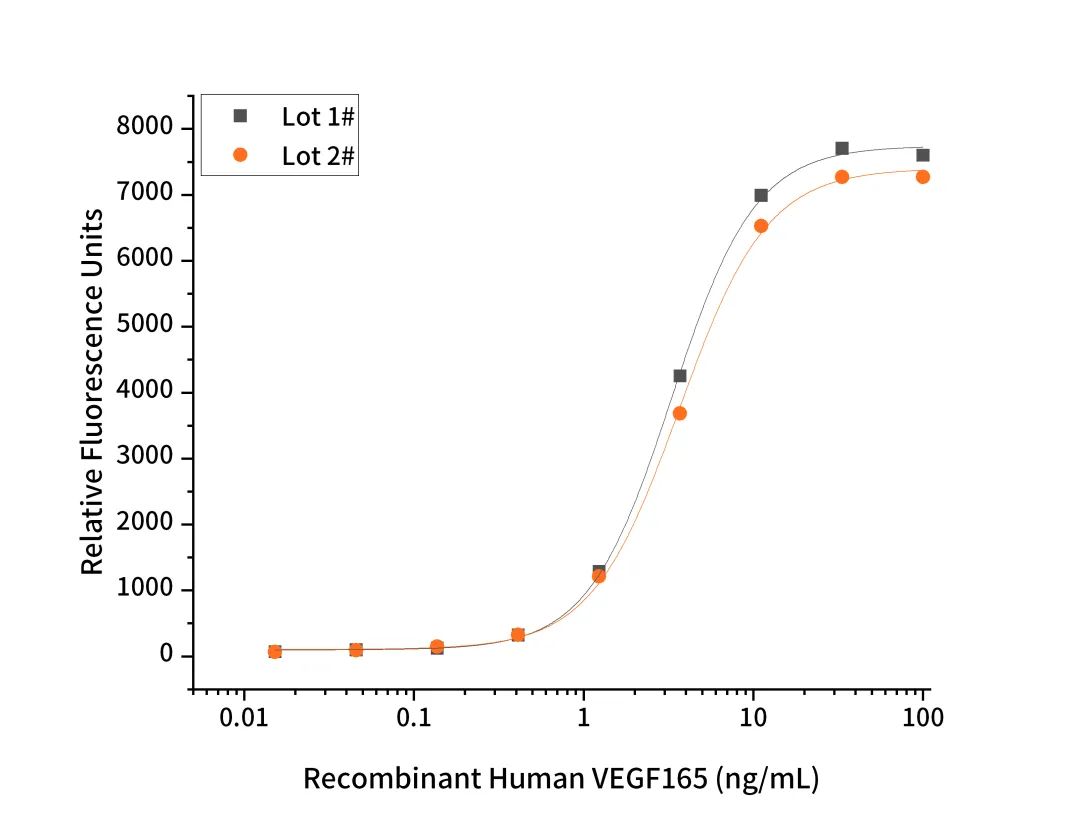
Measured by its ability to induce calcineurin- NFAT signaling in 293-VEGF Res cells. Two independent lots were tested for activity and plotted on the same graph to show lot-to-lot consistency of VEGF165.
血管生成相关细胞因子
|
|
|
|
|
|
|
|
|
GMP-CR96 |
Recombinant Human VEGF165 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
参考文献
[1]Apte RS, Chen DS, Ferrara N.VEGF in Signaling and Disease: Beyond Discovery and Development.Cell. 2019;176(6):1248-1264. doi:10.1016/j.cell.2019.01.021.
[2]Quan R, Du W, Zheng X, Xu S, Li Q, Ji X, Wu X, Shao R, Yang D. VEGF165 induces differentiation of hair follicle stem cells into endothelial cells and plays a role in in vivo angiogenesis. J Cell Mol Med. 2017 Aug;21(8):1593-1604. doi: 10.1111/jcmm.13089.
[3]Abutaleb, & Truskey, G. A. (2021). Differentiation and characterization of human iPSC-derived vascular endothelial cells under physiological shear stress. STAR Protocols, 2(2), 100394.
[4]Abilez OJ, Yang H, Guan Y, et al. Gastruloids enable modeling of the earliest stages of human cardiac and hepatic vascularization. Science. 2025;388(6751):eadu9375. doi:10.1126/science.adu9375
